|
Retour Histoire de science - page d'accueil, cours lycée, panorama |
|
|
|
|
||||||||||||||
|
|
|
Cette page s'efforce de présenter, avec le regard un peu synthétique du pédagogue, quelques évolutions du concept de cellule, et quelques incursions au-delà de ce concept, en ce début de XXIème siècle. Les simplifications faites, et les prospectives explorées, ne rendent peut-être pas justice aux idées plus nuancées des chercheurs. Comme la vulgarisation, l'enseignement expose l'auteur. Je suis très attentif à toutes les remarques que les lecteurs veulent bien m'adresser. |
||||||||||||||||
|
|
|
Sources
générales: |
|
Page
personnelle de
recherche
(biologie
théorique
thomienne) sur
l'hydratation Un site à recommander avec des vidéos et un texte clair :http://www.cerimes.fr/e_doc/cellule/cellule.htm |
||||||||||||||
|
|
|
|
||||||||||||||||
|
Plan |
|
|
|
Le
symbole |
||||||||||||||
|
|
|
|
||||||||||||||||
|
1. La théorie cellulaire, un produit de l'imagination du discontinu* |
||||||||||||||||||
|
|
* « La théorie des molécules organiques illustre une méthode d'explication, la méthode analytique, et privilégie un type d'imagination, l'imagination du discontinu .» (G. Canguilhem) |
|
G. Canguilhem attribue ainsi à Buffon une certaine paternité de la théorie cellulaire et cite : «... la vie étant dans chacune des parties, elle peut se retrouver dans un tout, dans un assemblage quelconque de ces parties. » (Buffon, Histoire des Animaux, chapitre X); |
|
Histoire
: la
théorie
cellulaire
|
|||||||||||||
|
|
|
|
La théorie fibrillaire, dans laquelle on peut voir un précurseur de la théorie cellulaire, correspondait au même imaginaire du discontinu. |
|||||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
La théorie cellulaire (Buffon, Oken, Vischov) comprend deux affirmations : |
|
*
tout
être
vivant est
composé
en
totalité
(et
uniquement)
d'au moins une
cellule |
||||||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
G.
Canguilhem
y ajoute deux
axiomes |
|
*
les vivants
non
composés
sont
unicellulaires
(Dujardin,
Haeckel) |
||||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
La cellule vivante n'est pas plus une chambre (cellula en latin), qu'une solution aqueuse, ni encore qu'une unité d'un programme du vivant. Une cellule est tout simplement un moyen commode que scientifiques et philosophes ont trouvé pour décrire le vivant: un concept qui désigne l'unité structurale et fonctionnelle du vivant. La cellule comme unité de structure découle du premier axiome de la théorie (tout être vivant est composé d'au moins une cellule). La cellule comme unité fonctionnelle est le plus petit élément VIVANT, qui possède TOUTES les caractéristiques du vivant. Si on reprend la formulation qui m'est chère, c'est la plus petite unité AU TRAVAIL: plus petite unité qui réalise un travail de nutrition, de relation et de reproduction. Le deuxième axiome de la théorie cellulaire (toute cellule est issue d'une autre cellule) permet de repousser la question de la vie hors du champ biologique et vers le champ philosophique, mais n'est pas une réponse en elle-même. La biologie doit se contenter de cette propriété du vivant qu'elle ne peut relier à aucun objet sans sortir de sa méthode (qui est expérimentale et qui ne peut répondre à la question de la vie). |
|
|
||||||||||||||
|
|
|
1ère
étape: La vision de René Thom s'est progressivement imposée à moi comme étant une réponse très pertinente à la recherche de propriétés locales, expérimentables, issues de propriétés générales, non locales. L'unité du vivant est alors à exprimer avec des objets mathématiques. Quand à l'unité structurale, elle repose alors sur le continu chimique de la cellule (l'eau étant en première ligne). |
|
2ème
étape: J'en suis donc revenu inconsciemment au deuxième axiome de la théorie cellulaire qui est en fait la source de la définition de l'espèce: « toute cellule est issue d'une autre cellule» devient: « tout être vivant hérite de la forme de son espèce par sa naissance à partir d'un être vivant de la même espèce.» La dimension évolutive comprise dans la théorie cellulaire devient apparente mais elle n'a de sens qu'au niveau de l'individu et non pas de la cellule. |
||||||||||||||
|
|
|
|
||||||||||||||||
|
2. Vers une théorie de l'organisme vivant relevant de l'imagination du continu : ondes, champs, gradients et fonctions du vivant |
||||||||||||||||||
|
|
G. Canguilhem, dans son analyse de la théorie cellulaire, souligne l'ambivalence "continu-discontinu (1)" sans cesse présente, même chez ceux que l'on considère comme les pères de la théorie cellulaire. L'aspect continu peut se rapporter à l'apparition des nouvelles cellules au sein d'un liquide formateur initial (que l'on peut rapprocher d'une matière continue : protoplasma d'Hugo von Mohl, cytoblastème de Schwann...), alors que l'aspect discontinu se retrouve dans les formes observées, assemblages de parties ou molécules (théorie des molécules organiques de Buffon...). |
|
|
|||||||||||||||
|
|
|
Je
vais suivre la
chronologie
avec trois
étapes
historiques
dans cette
marche vers le
continu: |
||||||||||||||||
|
|
|
2.1 L'eau du vivant, structurante et fonctionnelle le contenu de cette partie reprend essentiellement une ancienne page: l'eau dans la cellule à partir des travaux de Pascale Mentré |
||||||||||||||||
|
|
|
Sources
de cette
partie: |
|
Un site en anglais (de Martin Chaplin) particulièrement riche: http://www.lsbu.ac.uk/water/index.html Une page de culture générale sur l'eau |
||||||||||||||
|
2.1.1 Voir et imaginer l'eau de la matière vivante |
|
|
||||||||||||||||
|
|
|
Nous nous intéresserons à l'eau au niveau de la matière vivante que nous appellerons parfois eau cellulaire, même si notre but avoué est de nous affranchir du concept de cellule. |
||||||||||||||||
|
|
|
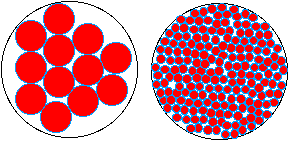
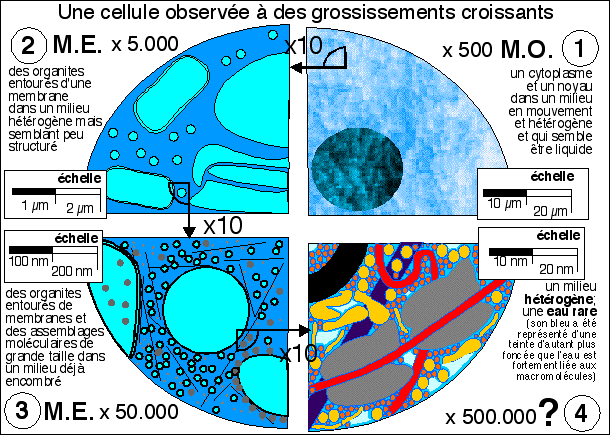
Ce schéma tente de montrer comment on est passé, grâce à l'évolution des techniques d'observation, d'une eau cellulaire majoritairement liquide, à une eau cellulaire sous des états variés, l'eau liquide étant très rare. |
||||||||||||||||
|
Ce
schéma
est assez
personnel et
je suis intéressé
par toute
remarque
à son
sujet |
|
 |
||||||||||||||||
|
|
|
le microscope optique (M.O. - 1) ne permet guère que de voir le noyau et le cytoplasme dont le contenu nous paraît clair mais hétérogène (un peu grumeleux). On peut aussi entr'apercevoir de gros organites comme des vacuoles, des chloroplastes ou des mitochondries. On peut colorer la cellule sans la tuer et voir par exemple les chloroplastes se déplacer entraînés par les mouvements du cytoplasme. |
|
Au microscope électronique (M.E. 2 et 3) la cellule est morte et fixée. Les structures ne sont pas vivantes mais mortes. De plus, on ne voit que celles qui fixent le colorant utilisé (tétroxyde d'osmium). On observe cependant une grande variété de structures. En 2 on distingue des mitochondries, des vésicules et les citernes du réticulum. En 3 les plus gros assemblages protéiques apparaissent comme les ribosomes et les microfilaments du cytosquelette. |
|
L'étape 4 n'est pas vraiment accessible à la microscopie pour des structures complexes en place mais représente ce que l'on peut imaginer être la réalité à partir d'observations de quelques éléments réellement observés mais isolés de la cellule et d'autres structures. |
||||||||||||
|
|
|
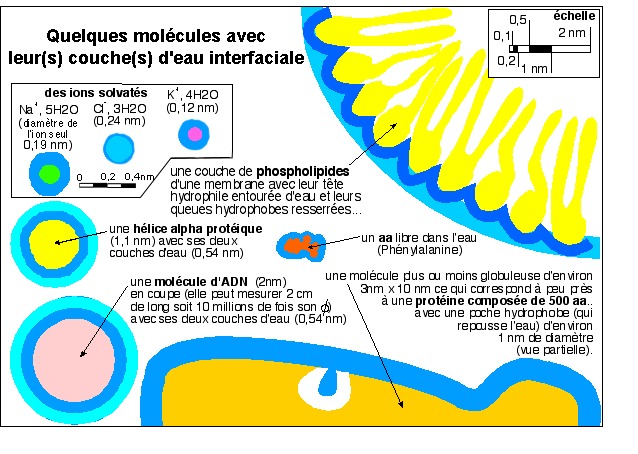
On reconnaîtra (en 4) en partant du coin gauche et en se déplaçant en diagonale vers le bas à droite: une vésicule dont la membrane (en noir) est une structure de près de 8 nm d'épaisseur, des macromolécules (en jaune) avec leur(s) couche(s) d'eau liée (les plus grosses protéines globulaires atteignent typiquement 5 nm de diamètre), un microfilament fin dessiné en arrière plan (en violet, leur diamètre varie de 5 nm pour les plus fins à 25 nm pour les plus épais), deux ribosomes (en gris, de diamètre environ 20 nm) autour d'un ARNm (en rouge, un filament de diamètre inférieur à 2 nm qui est le diamètre de la molécule d'ADN); les molécules organiques plus petites (de diamètre voisin du nanomètre - pensez qu'un aa comme la phénylalanine atteint déjà le nanomètre si l'on tient compte de sa couche d'eau liée - voir plus bas) avec leur(s) couche(s) d'eau liée encombrent le hyaloplasme; l'eau "libre" (en bleu clair) est rare et concentrée dans certains espaces. Pour des données sur la structure de la matrice cytoplasmique (ou cytomatrix en anglais) voir la Des
résultats
fondamentaux
sur le
cytosquelette
(au sens
large) de la
cellule sont
aussi
disponibles
dans l'article
Sheldon Penman
: Repenser
la structure
de la cellule.
Revue
de 1995 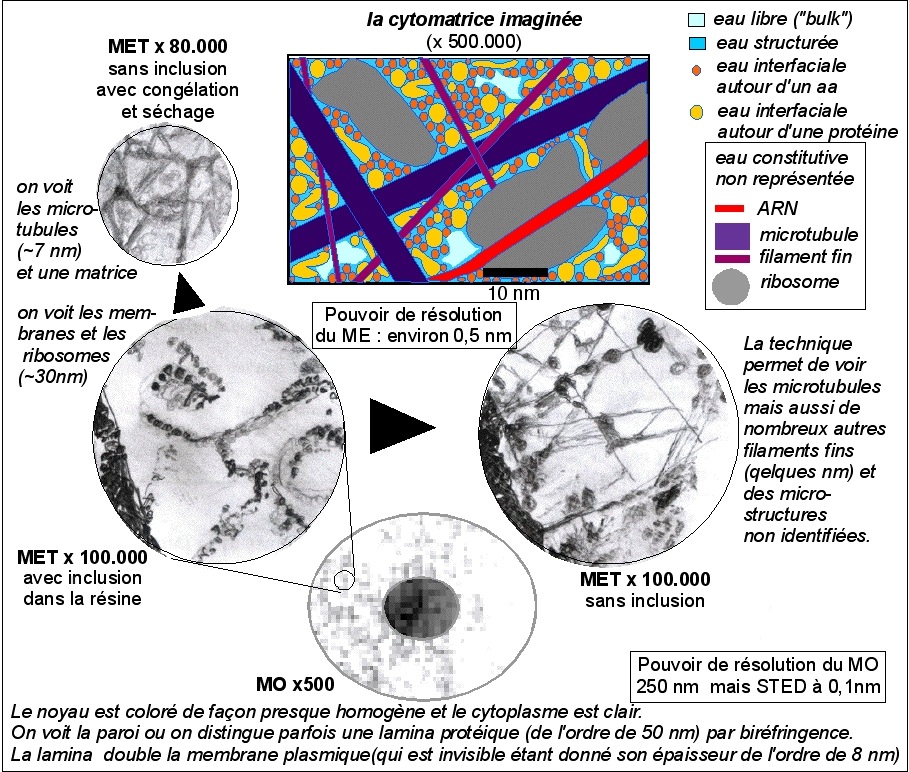 Les matrices extracellulaires et notamment les matrices intercellulaires des organismes pluricellulaires sont toutes des produits de la sécrétion des cellules, spécialisées ou non. Voir ici un tableau comparatif réalisé pour le nouveau programme de la classe de seconde. 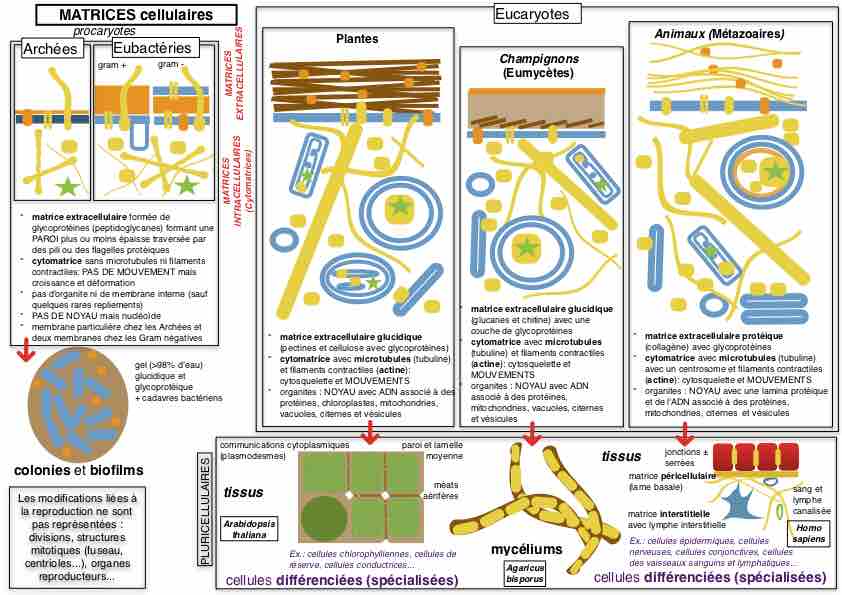 |
||||||||||||||||
|
|
|
|
|
si
20% de l'eau
de la
matière
vivante est
une eau libre, Si l'eau représente près de 80% en masse de la cellule vivante, cette eau est à près de 80% sous forme d'un film interfacial d'environ 1,1 nm d'épaisseur qui se trouve entre les molécules organiques structurant la cellule. Il reste donc 20% d'eau libre où s'appliquent les lois de la chimie des solutions aqueuses, principalement de l'eau présente dans des vésicules. |
||||||||||||||
|
|
|
a - Exemple: l'eau de l'ADN |
|
80% de la masse de l'ADN (extrait) est due à l'eau |
||||||||||||||
|
|
|
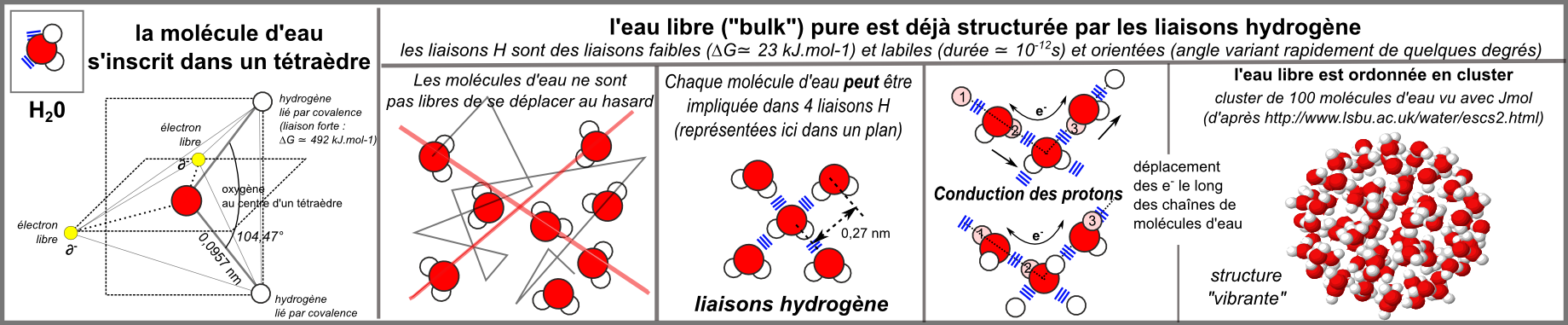
Pour comprendre comment une augmentation de la surface de contact, qui est due à la faible taille des macromolécules, augmente considérablement le volume d'eau associé à un ensemble de macromolécules, on peut prendre l'exemple de l'ADN: à chaque nucléotide est associé environ 20 molécules d'eau (eau "liée", très structurée, non congelable) ce qui représente environ 80% du poids de la molécule d'ADN. Si l'on place de l'ADN cristallisé en solution aqueuse il gonfle, ce que l'on peut expliquer par la mise en place d'au moins une seconde couche d'eau entre les brins d'ADN, couche moins structurée et congelable, dont l'origine pourrait provenir du caractère fortement électrolytique de la molécule d'ADN. Dans une cellule vivante, l'eau associée à l'ADN atteint ainsi une masse nettement supérieure à la masse d'ADN. On peut donc comprendre que, tout comme ses composants moléculaires, dont la forme est à la fois stabilisée par l'eau et due en partie à cette hydratation, la cellule contient une énorme quantité d'eau, fortement structurante et structurée. |
||||||||||||||||
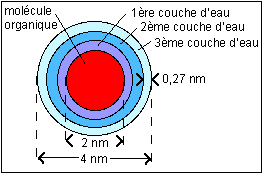 L'ADN, une molécule très hydratée |
|
Pour une molécule organique de 2 nm de diamètre (de l'ordre de celui de la molécule d'ADN qui est plutôt grossièrement cylindrique) supposée sphérique (donc de volume 33,5 nm3), une couche d'hydratation dont l'épaisseur est estimée à 0,27 nm correspond à un volume de (4/3 π (2,273-23)nm3= 15,5 nm3 ) soit un volume relatif de (2,273-23/23 ) soit 46%. |
|
Avec une
deuxième
couche d'eau
on atteint 105
% et
enfin 177%
avec une
troisième
couche d'eau. |
||||||||||||||
 |
||||||||||||||||||
|
|
|
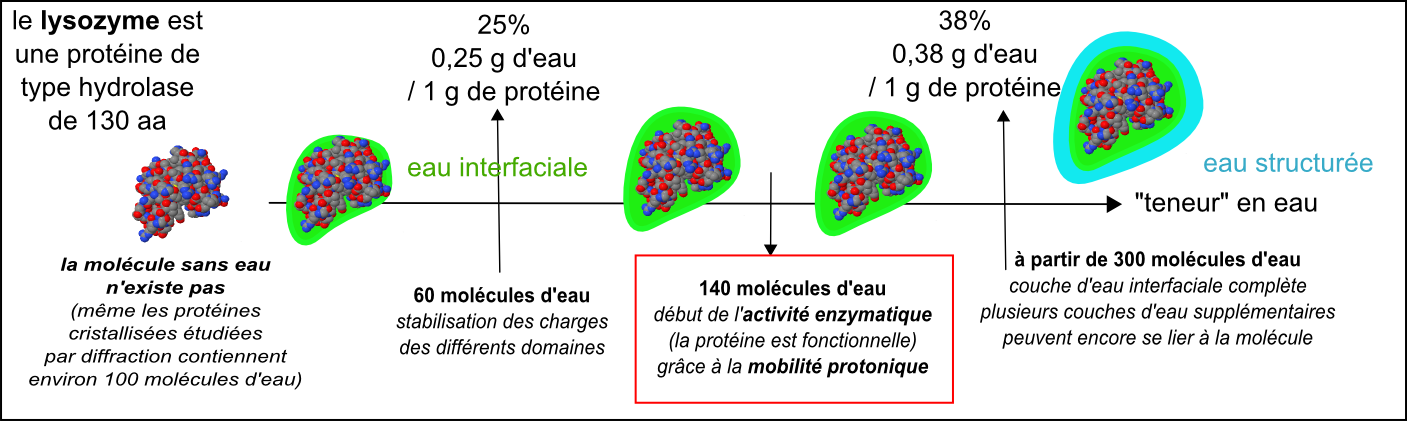
b - Généralisation: eau liée, eau structurée et eau libre |
|
|
||||||||||||||
|
|
|
Il est évident que, si la majorité des scientifiques actuels s'accordent pour la présence d'une couche d'eau "liée", l'épaisseur de la "coquille d'hydratation" est fortement discutée par les spécialistes. |
|
La
première
couche d'eau
est
appelée
eau
liée
(bound
water). |
|
Enfin il existe aussi une eau constitutive des macromolécules, inextractible sans modifier profondément la structure et la fonction de la molécule. |
||||||||||||
 |
||||||||||||||||||
|
|
|
c - Petits calculs pour comprendre |
|
|
||||||||||||||
|
|
|
En sachant
que
l'empilement
de
sphères
le plus dense
atteint
près de
75% du volume
total (c'est
la fameuse
conjecture de
Kepler qui a
reçu
une
démonstration
faisant
intensément
appel à
l'informatique
par Hales en
1999),
on peut faire
entrer
approximativement,
dans un volume
Vo
donné
d' environ 70
µm3,
100 sphères
de 1
micromètre
(1 µm)
de
diamètre,
possédant
une couche
d'eau
liée
environ 1,1 nm
d'épaisseur
ou 73 millions
de
sphères
d'un
diamètre
100 fois plus
petit (10 nm)
avec une
couche d'eau
liée de
la même
épaisseur. |
|
|
||||||||||||||
|
|
|
Cette analogie géométrique peut aider à comprendre comment une cellule contiendrait 80% de son eau sous forme d'eau interfaciale (liée) constituant un microfilm de 1,1 nm d'épaisseur autour des macromolécules cellulaires. 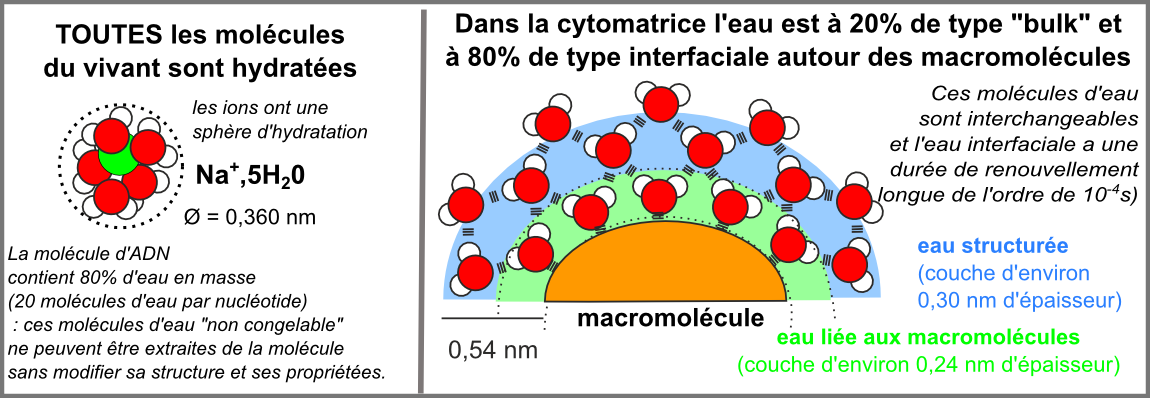 |
||||||||||||||||
|
|
|
|
|
le
cytoplasme
n'est pas un
milieu - un
solvant plus
ou moins
liquide - de
molécules
en solution
... |
||||||||||||||
|
|
|
d - L'eau interfaciale de quelques molécules |
|
|
||||||||||||||
|
|
|
Même si les spécialistes discutent pour savoir quel est le nombre habituel de couches d'eau liée autour des macromolécules, elles sont omniprésentes. Une molécule est toujours entourée d'eau plus ou moins fortement attachée à elle. Cette eau est ordonnée selon les interactions qu'elle développe avec la molécule à laquelle elle se lie: on parle ainsi d'eau liée ou d'eau structurée. Par rapport à la figure 1, cette figure correspondrait à un grossissement environ dix fois plus fort le grossissement le plus fort de la figure 1 soit environ 5.000.000 de fois; ce qui n'est bien sûr pas accessible à une quelconque technique microscopique sur des molécules en place dans un cytoplasme, et encore moins sur de la matière vivante. Nous devons donc nous contenter d'interprétations, réalisées par des méthodes indirectes, et non d'observations. |
||||||||||||||||
|
|
|
e - Quelques formes de l'eau interfaciale (un peu plus de chimie): |
|
|
||||||||||||||
|
|
|
- les molécules d'eau établissent des liaisons hydrogène entre elles (structure ice-like) qui sont fortement favorisées dans les poches hydrophobes et au voisinage des domaines apolaires des molécules; |
|
- les molécules d'eau (polarisées) sont fortement attirées par les domaines ionisés des molécules et forment une eau électrostrictée dont la densité peut atteindre 1,2. Les molécules d'eau électrostrictée s'échangent sans cesse avec l'eau bulk; |
|
- les molécules d'eau sont fortement immobilisées par des liaisons hydrogène (de structure variées) au niveau des domaines polaires. |
||||||||||||
|
|
|
|
||||||||||||||||
|
|
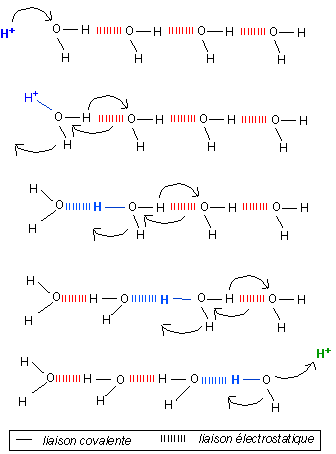
La petite taille du proton est à l'origine de l'intensité de la liaison hydrogène car un champ électrostatique engendré par une particule de charge q varie en q/d2, si d est la distance au centre de la particule. Le proton forme un pont entre un atome donneur auquel il est lié de façon covalente (O) et un atome accepteur qu'il attire électriquement (O ou N, mais aussi C ou encore un nuage d'électrons π d'un cycle aromatique...) . |
|
L'habituelle linéarité de la liaison hydrogène observée entre molécules d'eau dans la glace, n'est pas conservée dans toutes les liaisons hydrogène qui peuvent aussi présenter des énergies variables en fonction de leur longueur (8 kJ.mol-1 pour les plus courtes liaisons à 42 kJ.mol-1 pour les liaisons les plus longues). L'établissement d'une liaison hydrogène modifiant les caractéristiques du donneur et de l'accepteur, on observe un phénomène de coopérativité qui facilite l'établissement de liaisons en chaîne. Ces chaînes de molécules d'eau liée expliqueraient nombre de fonctions de l'eau interfaciale. |
|||||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
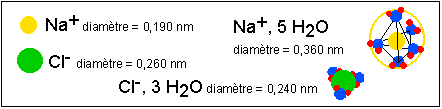
La solvatation résulte de l'établissement de liaisons électrostatiques entre les molécules d'eau et les ions et de liaisons hydrogène entre les molécules d'eau de cette "couche" dite de solvatation. Le nombre moyen de molécules d'eau de la couche de solvatation dépend de la charge de l'ion et de son rayon atomique: plus l'ion est chargé plus il attire les molécules d'eau; et à charge égale, plus un ion a un rayon ionique important, moins il attire de molécules d'eau. |
||||||||||||||||
|
|
|
Pour un ion de grande taille de charge négative comme le chlore, cette charge est répartie sur toute la surface de l'ion (1/S=1/π R2) est est donc plus faible que pour un ion de petite taille comme de sodium. Ainsi l'ion chlorure est solvaté par environ 3 molécules d'eau pour un rayon de solvatation inférieur au rayon de l'ion dans un solide ionique (NaCl) alors que l'ion sodium est solvaté par environ 5 molécules d'eau et son rayon ionique est presque deux fois plus faible que lorsqu'il est solvaté. |
|
Un autre exemple est le lithium (ion Li+) qui est solvaté par environ 6 molécules d'eau ce qui fait passer son rayon ionique de 0,060 nm à 0,236 nm (soit près de 4 fois plus) lorsqu'il est solvaté. L'ion potassium (K+), volumineux, et ne portant qu'une seule charge positive, n'est solvaté que par 4 molécules d'eau en moyenne, et passe d'un rayon ionique de 0,133 nm à 0,121 nm lorsqu'il est hydraté. |
|
Dans un champ électrique, EN SOLUTION, les ions les plus petits et les plus solvatés migrent le plus lentement. |
||||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
Les clathrates sont des structures polyédriques à faces pentagonales qui contiennent des molécules d'eau réunies par des liaisons hydrogène et des molécules hydrophobes (on connaissait les clathrates en géologie où c'est une forme d'association de l'eau avec les hydrocarbures, et en astrophysique où ces structures ont été utilisées pour expliquer certaines caractéristiques spectroscopiques des rayonnements de certaines corps célestes) . |
||||||||||||||||
|
|
|
Les
clathrates
sont
très
stables,
cristallisables,
et peuvent
contenir
jusqu'à
90% d'eau. |
||||||||||||||||
|
|
|
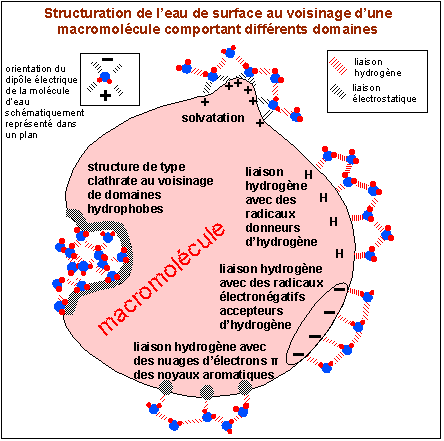
Les 3 types principaux de structuration de l'eau au voisinage d'une macromolécule: eau de solvatation (remarquez la seconde couche d'eau liée à la première par des liaisons hydrogène: la première couche est appelée eau liée (sous-entendu à la macromolécule), la seconde, eau structurée), eau liée par des liaisons hydrogène à des domaines polaires ou à des nuages d'électrons π (là aussi une seconde couche d'eau stabilise la première couche), eau liée par des liaisons hydrogène en structures de type clathrate au voisinage de domaines hydrophobes (d'après Mentré, 1995, Fig 12.2 principalement). |
||||||||||||||||
|
|
|
|
|
l'eau de la matière vivante est très hétérogène * elle est polarisée (anisotrope), * elle présente des variations importantes dans son architecture, son degré de coopérativité et sa densité, * elle possède un pouvoir solvant réduit, * elle possède une activité osmotique réduite. |
||||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
f - C'est l'eau qui structure le vivant et non pas les membranes |
|
|
||||||||||||||
|
|
|
|
|
les états de l'eau chez les êtres vivants |
||||||||||||||
|
Sommairement on peut distinguer: |
|
* un milieu
thixotropique
(avec
à la
fois des
propriétés
de solide et
de liquide)
: la matière
vivante
(c'est
l'ancien
contenu
cellulaire ou
tissulaire :
parenchyme,
muscle,
épithélium,
os...), avec
60 à
90% d'eau dont
environ 20%
correspond
à de
l'eau libre et
80% à
de l'eau
interfaciale |
|
* des barrières : les parois, mucilages et autres milieux d'échanges dont le contenu en eau libre est réduit mais pour lesquels la mobilité est forte |
|
* des
fluides:
les
liquides
(plasma,
sèves...)
et les gaz
(avec des
goutelettes et
microgoutellettes
d'eau) qui
sont des
milieux
particuliers
où
l'eau liquide
libre est la
phase
dominante. |
||||||||||||
|
|
|
|
|
quels rôles pour les membranes ? |
||||||||||||||
|
|
|
|
||||||||||||||||
|
Je signale
ici au passage
la vision de Sheldon
Penman
dans son
article Repenser
la structure
de la cellule.
Revue
de 1995 |
|
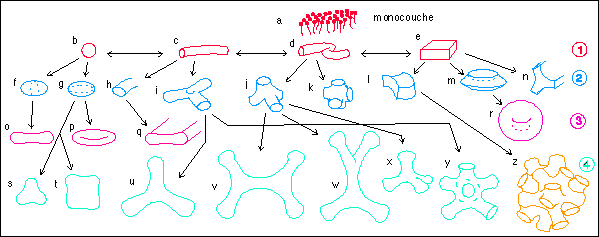
Les
membranes
monocouches
ont une face
hydrophile et
une face
fortement
hydrophobe.
Elles ont
tendance
à
former des
micelles au
centre
hydrophobe et
à
l'extérieur
hydrophile. |
|
Une interprétation particulièrement astucieuse de la topologie des membranes a été présentée par d'Yves Bouligand (sur l'ancienne page sur les modèles) je recommande particulièrement la figure présentant Une "microzoologie" des formes observées et supposées de micelles "membranaires" ).ci-contre------------> |
|
 |
||||||||||||
|
|
|
|||||||||||||||||
|
|
Mais les membranes ne perdent pas pour autant leurs rôles dans la communication, mais plutôt que d'interfaces (cellulaires), elles pourraient servir de surfaces communicantes entre espaces dynamiques plus ou moins éloignés : des cosurfaces |
|
|
|||||||||||||||
|
|
Jean-Pierre Miolan : « Un nouveau mode de conduction des signaux nerveux », La Recherche, 413, nov 2007, 14-15
|
|
Les membranes, notamment des neurones, pourraient servir de surfaces communicantes par le biais de microdomaines lipidiques: des radeaux (rafts en anglais) de sphingolipides . Le mécanisme proposé par cette équipe fait intervenir l'activation en cascade d'une séquence de seconds messagers dont certains comme le céramide sont situés dans les radeaux. Il permettrait une vitesse de conduction du signal de l'ordre du cm à la minute. On notera bien que c'est l'activation des seconds messagers qui se déplace et non les radeaux. Caroline Fasano, Jean-Pierre Miolan et Jean-Pierre Niel travaillent depuis un certain temps sur les sphingolipides membranaires; voir un article dans Médecine sciences accessible et en français: Les sphingolipides : vecteurs d'agents pathogènes et cause de maladies génétiques, Médecine/Science, avril 2006, 22, 4 |
|
article original en anglais: Fasano C, Tercé F, Niel JP, Nguyen HTT, Hiol A, et al. (2007) Neuronal Conduction of Excitation without Action Potentials Based on Ceramide Production. PLoS ONE 2(7): e612 doi:10.1371/ journal.pone.0000612 |
|||||||||||||
|
|
|
(en travaux) |
||||||||||||||||
|
2.1.2 Les fonctions de l'eau |
|
|
||||||||||||||||
|
|
|
L'eau n'est
donc plus
seulement constitutive
du vivant
(matière
vivante,
milieu de vie)
mais ses rôles
se
découvrent
aussi énergétiques
(mécaniques,
chimiques...)
et relationnels. |
||||||||||||||||
|
|
|
a - L'eau cytoplasmique n'est pas un solvant mais est organisée |
|
|
||||||||||||||
|
* mais il existe d'autres gradients beaucoup plus pertinents: le gradient c'est la dérivée d'une fonction: une telle fonction ne peut s'appuyer sur des atomes et des molécules, elle doit provenir d'un champ qui n'est pas déterminé par des particules : champ de nutrition par exemple. |
|
|
|
les concentrations in vivo sont trop faibles pour obéir aux lois de la chimie des solutions: la notion de gradient* de concentration perd tout sens dans une cellule: |
||||||||||||||
|
|
On estime qu'une bactérie comme Echerichia coli ne contient qu'une centaine de protons qui sont éloignés les uns des autres de plusieurs centaines de nm et donc ne peuvent être responsables d'un gradient de concentration. De même pour les ions calcium que l'on estime à une concentration cellulaire de 10-3M dont 10-8M à 10-6 libres (non complexé par des macromolécules comme la calmoduline...) mais solvaté (entouré par des molécules d'eau). |
|
|
|||||||||||||||
|
|
|
Comment imaginer qu'une dizaine d'ions ou même quelques milliers d'ions, séparés par de très nombreuses macromolécules puissent déterminer un gradient de concentration à de telles distances ! Quand aux compartiments membranaires habituellement invoqués pour présenter une concentration homogène, leur taille étant de l'ordre de la centaine de nanomètre (épaisseur d'une citerne golgienne ou du réticulum endoplasmique) au micromètre (mitochondrie), ils ne peuvent non plus contenir plus de quelques unités à dizaines d'unités de ces ions, bien incapables donc de déterminer un gradient de concentration. Cette remarque d'une part remet en cause probablement la mesure des concentrations aussi faibles que celles présentées et d'autre part oblige à considérer que les molécules sont avant tout liées à d'autres molécules dans la cellule et que l'eau ne joue que très rarement, le rôle de solvant. |
||||||||||||||||
|
|
|
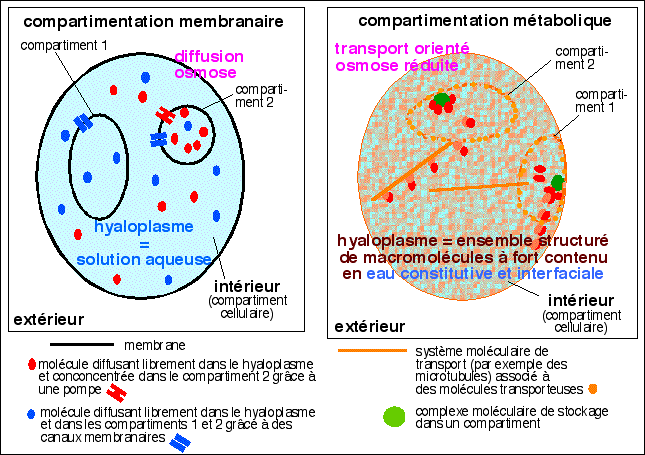
Les concentrations extrêmement faibles estimées pour le vivant conduisent à des interprétations trompeuses si l'on pense que le compartiment cellulaire bactérien, par exemple, est un milieu homogène où la chimie des solutions en milieu aqueux pourrait s'appliquer. Ainsi une concentration en calcium de 10 nanomoles correspond à environ 12 ions calcium dans le cytoplasme. Avec des chiffres aussi petits il est indispensable d'envisager une chimie des milieux hétérogènes pour le cytoplasme dont une représentation très imagée est proposée. On reconnaîtra la membrane plasmique (en orange) avec des protéines membranaires (en jaune) , des ribosomes (en gris) et des éléments du cytosquelette (en violet). Le calcium libre est très probablement séquestré dans des microdomaines très localisés (en bleu foncé) dans lesquels on peut peut-être utiliser une chimie statistique avec par exemple la loi d'action de masses, mais il est incohérent de l'appliquer à l'ensemble du compartiment cellulaire. |
||||||||||||||||
|
|
|
|
|
les propriétés physiques du cytoplasme, sont hétérogènes et très variables selon les types de cytoplasmes dans les différents tissus, ce qui peut notamment être expliqué par les différentes formes de l'eau au sein de ce cytoplasme |
||||||||||||||
|
|
|
Le
hyaloplasme ne
formerait pas
une
entité
homogène
au
comportement
physique
identique sauf
dans quelques
cellules
très
spécialisées
comme les
hématies
dont la
compartimentation
est
réduite
à un
quasi-unique
compartiment,
monofonctionnel.
L'immense
vacuole des
cellules
végétales
peut aussi
constituer un
bon exemple de
compartiment
d'une telle
homogénéité. |
|
Une des
théories
les plus
séduisantes
sur
l'organisation
de l'eau
cytoplasmique
est la théorie
de Watterson
(1982,1991);
la tension
existant dans
un volume
d'eau est
reliée
par l'auteur
aux mouvements
vibratoires
des
molécules
qui seraient
dus aux
phénomènes
de
coopérativité
(résonance)
observés
entre les
molécules
d'eau
reliées
par des
liaisons
hydrogène. |
|
Un point essentiel d'application de cette théorie est que la plupart des protéines intracytoplasmiques ont des dimensions qui correspondent précisément à un cluster: 40 nm3 pour un nombre de résidus compris entre 120 et 300 et un diamètre moyen de 3,5 nm. Ces clusters ne seraient pas des structures rigides mais dynamiques, très sensibles aux éléments introduits; les protéines polymériques par exemple, d'une taille supérieure à un cluster, modifiant la résonance de l'ensemble. Watterson propose de relier la stabilité de la matrice hyaloplasmique à l'harmonie vibratoire des domaines d'eau et de macromolécules entourées d'eau. La cohérence résultant alors non pas de forces de liaison mais de mouvements vibratoires résonnants, sensibles aux perturbations (et permettant ainsi de transférer extrêmement rapidement un signal (modification de la longueur d'onde...) d'un point à un autre) mais résistants grâce à leur souplesse. |
||||||||||||
|
|
|
|
|
paradoxalement, l'eau du cytoplasme vivant - surpeuplé de macromolécules - devient rare, étant utilisée de façon compétitive par les macromolécules; son accessibilité contrôle alors les activités des biomolécules |
||||||||||||||
|
|
|
Un excès d'eau impliquerait un désordre par manque de structuration. Un (léger) déficit d'eau entretient la possibilité d'un contrôle par facteur limitant. |
|
Pour étudier cette hypothèse P. Mentré et G. Hui Bon Hoa ont étudié des biomolécules sous haute pression hydrostatique (HPH), facteur connu pour favoriser une forte hydratation de ces molécules et donc une configuration qui maximise l'eau interfaciale, plus dense (d'après la loi de Le Chatelier). |
|
Les résultats obtenus sur des cellules eucaryotes - qui semblent pouvoir supporter sans problème des pressions atteignant 1000 à 1200 bars (soit 100 à 120 MPa) pendant une dizaine de minutes - sont époustouflants : cytosquelette, complexes antigène-anticorps, ADN-facteurs, etc., se dissocient sous des HP de quelques dizaines de MPa et cet effet est réversible. Le contrôle des assemblages biomoléculaires par l'eau est en voie d'exploration. |
||||||||||||
|
|
||||||||||||||||||
|
|
|
b - L'eau canal de transport et de communication |
|
|
||||||||||||||
|
|
|
|
|
L'eau n'est pas immobile mais percole le cytoplasme |
||||||||||||||
|
|
|
Toutes les liaisons évoquées ci-dessus sont des liaisons dynamiques dont le turn-over est rapide. Une molécule d'eau engagée dans une liaison électrostatique avec un domaine ionisé d'une molécule reste moins longtemps dans cet état que dans l'eau bulk qu'elle rejoint au bout de quelque temps. L'eau interfaciale peut aussi se déplacer avec les structures cellulaires qu'elle enrobe, et ce, avec des vitesses bien supérieures à celle de la diffusion dans une eau bulk. On peut considérer que les molécules de toute petite taille sont capables de percoler avec l'eau interfaciale. La plupart des macromolécules, qui sont d'ailleurs souvent associées en complexes moléculaires, sont transportées. |
|
Il n'en reste pas moins que ce que l'on nomme l'autodiffusion de l'eau dans la cellule reste un phénomène à explorer ( ce qui a déjà été commencé mais sort du cadre de cette synthèse partielle - voir Mentré,2002, p 103-104 et références) à la lumière de cette nouvelle vision de la cellule vivante. |
|
Le transport de l'eau par les vésicules de pinocytose reste aussi un mode de transport rapide et efficace. |
||||||||||||
|
|
|
|
|
les transports de molécules, d'ions, de signaux se font d'autant plus rapidement qu'ils sont associés à des structures de transport de grande taille |
||||||||||||||
|
|
|
Par exemple, au sein d'un axone, on estime la vitesse de diffusion de protéines isolées (de diamètre de l'ordre de quelques nm) inférieure à 0,01 µm.s-1, alors que avec des protéines transporteuses (de diamètre de l'ordre d'une dizaine de nm) on atteint des vitesses de l'ordre de 0,05 µm.s-1 et enfin, avec des vésicules (de l'ordre de 100 µm de diamètre) on atteint des vitesses de l'ordre de 0,5 µm.s-1. Pour chaque ordre de grandeur de taille on gagne un ordre de grandeur en vitesse (in Mentré, 2002, p 91). |
||||||||||||||||
|
|
|
|
|
les molécules d'eau liées forment un réseau subtil coordonateur |
||||||||||||||
|
|
|
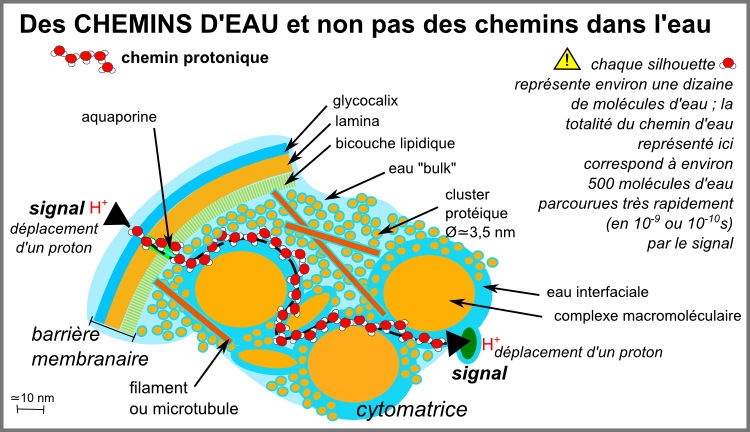
les chaînes de molécules d'eau, à la surface de macromolécules où reliant des molécules entre elles, présentent, comme dans la glace (mais avec une mobilité réduite cependant), une conductivité protonique efficace qui pourrait emprunter les circuits de conduction de l'eau interfaciale formant, selon l'expression de R. Peters un réseau subtil coordinateur. |
|
|
||||||||||||||
|
|
|
Conduction
protonique |
|
|||||||||||||||
 |
||||||||||||||||||
|
|
|
Cette conductivité est actuellement une piste majeure de recherche en biochimie,
|
||||||||||||||||
|
|
||||||||||||||||||
|
|
|
c - L'eau participe au métabolisme et le dirige peut-être |
|
|
||||||||||||||
|
|
|
|
|
le pouvoir régulateur de l'eau structurée |
||||||||||||||
|
|
|
La première couche d'eau interfaciale (eau liée) semble joue le rôle d'élément de contrôle principal, du fait notamment de sa forte coopérativité (elle est plus difficilement perturbable); la seconde couche étant surtout un réservoir. Mais les échanges entre ces deux couches (mécanisme appelé micro-osmose) sont eux-mêmes un élément essentiel du pouvoir régulateur de l'eau structurée en général. |
|
l'eau
interfaciale,
par ses
liaisons
multiples avec
des domaines
variés
des complexes
moléculaires
contrôle
leur
assemblage-désassemblage
et leur
fonctionnement. |
|
On peut aussi citer les nombreuses enzymes activées spécifiquement par le potassium et non par le sodium. Le contrôle de l'activité de ces enzymes serait directement due à l'eau interfaciale. En effet, le site catalytique des enzymes est généralement hydrophile mais situé la plupart du temps au fond d'une poche hydrophobe. Quand le substrat se lie au site de l'enzyme le caractère hydrophobe de la poche s'accentue ce qui tend à structurer davantage l'eau (ice-like). Cette structure à la propriété d'exclure fortement le Na+ mais non le K+ (voir deux paragraphes plus loin, l'utilisation de la série de Hofmeister). Les ions K+ entrent alors dans la poche et déstructurent l'eau (état vapor-like) qui augmente de volume. Cette effet mécanique entraînerait l'ouverture de la poche et la libération du produit de la réaction enzymatique (in Mentré, 2002, p 96, §3.2.2). |
||||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
l'eau
interfaciale,
comme son nom
l'indique, contrôle,
par sa
position, les
mécanismes
informationnels
supposant une
reconnaissance
moléculaire
(topologique). |
|
l'eau
interfaciale,
de par ses
propriétés
physiques,
peut
contrôler
la composition
chimique de
la cellule:
c'est par
exemple
l'exclusion
sélective
des ions.
|
||||||||||||||
|
|
|
|
Les ions chaotropes, à la différence des ions cosmotropes circulent facilement dans les couches d'eau qu'ils déstructurent. C'est une raison avancée pour expliquer que le potassium, contrairement au sodium n'est pas exclu de la cellule. Certains auteurs estiment que la plus forte concentration en potassium du hyaloplasme par rapport au sodium est une conséquence directe du pouvoir solvant sélectif de l'eau interfaciale et non le résultat d'une activité membranaire. On a même montré expérimentalement que des cellules, dont les membranes ont été perméabilisées par des détergents, et placées dans des milieux riches en sodium, calcium et magnésium, ne s'enrichissaient pas notablement en ces ions (alors que leur concentration ionique est faible pour ces ions). Par contre, ces cellules à membrane perméabilisée, placées dans un milieu riche en potassium (mais moins riche que la cellule), perdent rapidement leur potassium. |
|||||||||||||||
|
|
|
|
|
les réactions chimiques du métabolisme se font dans des structures complexes, sans eau libre, ce qui explique des rendements proches de 100% |
||||||||||||||
|
|
|
La faiblesse des rendements en solution aqueuse peut être due au peu d'accessibilité des substrats; l'excellent rendement pour des enzymes associées en complexe est dû à la diminution du temps de transit d'une enzyme à l'autre; on désigne ce mécanisme d'association par le terme de canalisation (chanelling) ou d'une façon plus générale de compartimentation métabolique qui exprime l'idée d'association des enzymes impliquées dans une même chaîne métabolique . |
|
La compartimentation métabolique est donc une notion qu'il faut étendre à la totalité de la cellule, en relativisant la notion de membrane et des canaux ou transporteurs qui lui étaient associés. Un compartiment métabolique peut très bien se répartir à la fois dans un organite, le long d'une membrane et à l'extérieur de celle-ci. |
|
L'eau structurée pourrait servir de réseau de coordination des signaux intracellulaires au sein de laquelle les transports seraient nettement plus rapide que dans une eau libre; des résultats assez convaincants ont déjà été obtenus avec des mouvements de protons qui transmettent des signaux extérieurs en signaux intracellulaires. |
||||||||||||
|
|
|
|
|
le pouvoir mécanosensible ou mécanogénérateur de l'eau par micro-osmose les déplacements d'eau depuis la seconde couche d'hydratation vers la première couche d'eau liée (mécanisme de micro-osmose) s'accompagnent de changements de densité, donc de volume, et induisent alors des effets mécaniques. |
||||||||||||||
|
|
|
Le
rôle de
ces
changements de
densité
dans les moteurs
moléculaires
a fait l'objet
de nombreuses
recherches. On
a notamment
proposé
(voir
références
d'Oplatka, in
Mentré,
2002 p
100-101)
l'existence de
minijets d'eau
à
l'interface
des
molécules
d'actine et de
myosine
associées
dans les
myofilaments
des cellules
musculaires.
Le glissement
relatif entre
les
myofilaments
serait du
à la
force
mécanique
de l'eau
déstructurée
projetée
sous forme de
minijets, ce
qui a fait
comparer le
mécanisme
de la
contraction
musculaire
ainsi
revisité
à un
moteur
alternatif
à
vapeur. |
|
Les effets mécaniques des changements de densité de l'eau structurée pourraient aussi rendre compte de la transduction de signaux notamment depuis la membrane jusqu'aux structures internes de la cellule par le biais du cytosquelette. Une déformation de la membrane cellulaire peut modifier par contrainte mécanique la structure de l'eau structurée au voisinage de cette membrane. Cette modification pourrait ensuite se transmettre, mécaniquement, de proche en proche, au sein de l'eau d'hydratation des éléments du cytosquelette que l'on sait se polymériser/dépolymériser à grande vitesse. On a ainsi mis récemment en évidence que 10 à 12 molécules d'eau s'associent à la molécule d'actine au cours de son étape de polymérisation. |
|
Remarque
personnelle 1: |
||||||||||||
|
|
|
2.2 Les phases du vivant : la physique de la vie ....encouragements à suivre de nouvelles pistes |
|
|
||
|
«... il y aurait lieu d'introduire de manière plus systématique la notion de "phase" : le tissu osseux est - à peu près - une réalisation de la phase solide ; le tissu sanguin réalise une phase liquide ; or chaque phase a son propre "groupe de symétrie" qui lui aussi agit dans l'espace u des coordonnées spatio-temporelles ; d'où des contraintes sur l'application de l'espace (u) dans le "déploiement" de la bifurcation, application qui définit la croissance et le mouvement de la phase correspondante. Les phases locales définies par des minima des potentiels V(x; u) seraient à la fois en équilibre "sémantique" - dans un champ sémantique approprié - et globalement, des contraintes de conservation des espèces chimiques et de leur ordre moléculaire imposeraient des relations entre les modes de croissance de ces phases (noter que le problème analogue de la croissance d'une phase en milieu inanimé - par exemple, une cristallisation - n'est pas résolu). On pourrait donc qualifier cette méthode de structuralisme dynamique ; elle réconcilie Geoffroy-Saint-Hilaire et Cuvier : Geoffroy, parce que la succession des différenciations successives dans l'embryon se réalise de manière sensiblement isomorphe entre diverses espèces de Vertébrés ; Cuvier, parce que les potentiels locaux V(x; u) (ou fonctions de Lyapunov) ont une signification fonctionnelle liée à la régulation globale de l'organisme. On a affaire là à une sorte de vitalisme méthodologique , nullement incompatible, d'ailleurs, avec le réductionnisme physico-chimique.» René Thom, 1981f11 |
|
Dynamique globale et morphologie locale chez les êtres vivants, 1981, 11. Preprint IHES, Bures-sur-Yvette, cf. ULP, Sém. Fond. Sc. RCP 443, Strasbourg, 13 novembre 1981). |
||||
|
|
|
|
||||
|
page complémentaire sur les modèles de la théorie des catastrophes page sur le continu |
|
La phase d'un système (au sens de la thermodynamique) est définie comme une partie homogène séparée des autres parties du système par une surface (EU, "Transitions de phase"). Mais cette surface est définie non pas dans notre espace de perception (euclidien, à trois dimensions: la longueur, la largueur, la hauteur) mais dans un espace de dimension souvent assez grande ou espace des phases où le système possède un état totalement défini à partir des ses coordonnées. |
|
On peut aussi dire que l'espace des phases est l'espace le plus simple qui permette de définir de façon précise l'état d'un système (voir page sur le continu). Cet espace possède comme coordonnées les variables dynamiques indépendantes du système. À tout instant le fait de connaître les coordonnées du système dans l'espace des phases permet de connaître son état (dynamique). Dans les lignes qui suivent le mot "phase" sera donc utilisé de façon indifférente pour désigner une étape d'un phénomène (le temps étant alors la variable principale) qu'un ensemble plus ou moins homogène matériel (une molécule, un tissu, un organe) ou immatériel (une surface, un volume...). |
|
Avec le vocabulaire aristotélico-thomien une phase c'est un anhoméomère (1987f9). Un système peut comporter une ou plusieurs phases. |
|
|
|
|
|
2.2.1. Les phases moléculaires et macromoléculaires |
||
|
|
Quelles
sont les
dynamiques
attachées
aux phases
moléculaires
? Voici un essai de présentation à partir de l'exemple de l'ADN. |
|
Les dynamiques sont en nombre fini. Elles sont contraintes par le lois de la matière.
|
|||
|
|
|
l'ADN est présent selon plusieurs phases correspondant à des dynamiques différentes L'ADN est une des macromolécules les plus étudiées. L'idée selon laquelle l'organisation structurale de la molécule dans l'espace et dans le temps (dynamique) pourraient contrôler ses fonctions est bien ancienne. L'idée, ici, serait de séparer les différentes formes de l'ADN que l'on rencontre dans la cellule (ou hors de la cellule) comme autant de phases et non plus comme un seul objet décrit par ses caractéristiques chimiques. La fonction, pour chaque phase, serait étroitement associée à la dynamique - ne pas oublier que l'on s'efforce ici de proposer un modèle continu et non une dynamique qui résulterait de la somme des dynamiques élémentaires de chaque composant (les molécules). La dynamique vient clairement d'ailleurs que de l'ADN. |
|
|
||
|
E.U. article "cristaux liquides" et tous les travaux d'Yves Bouligand; phases mésomorphes, myéliniques, smectiques et nématiques |
|
1er cas: 2ème cas: l'ADN, sous forme filamenteuse, est répliqué selon un processus enzymatique. La dynamique de réplication est enzymatique mais il ne s'agit pas uniquement de l'allongement d'une molécule, comme dans le cas déjà étudié de la traduction (voir la fonction ribosomiale), mais en même temps d'une séparation-réassemblage (une fente qui s'ouvre et se ferme). Le temps caractéristique est d'un ordre inférieur à la minute. |
|
On dit souvent que les acides nucléiques ne peuvent former seuls de grands assemblages macromoléculaires alors que les protéines le peuvent. C'est relativement faux puisque lorsque l'ADN n'est que peu entouré de protéines (bactéries, certains protozoaires, certains noyaux de spermatozoïdes...) on observe des phases dites cholestériques de filaments plus ou moins orientés. Ces phases sont de même nature que celles observées dans le cas des fibres de cellulose ou de collagène... |
|
Voir les travaux d'Yves Bouligand (EPHE, voir articles dans E.U.: phases mésomorphes, cristaux liquides) ou de Françoise LIVOLANT (Laboratoire de Physique des Solides, Université Paris Sud, Orsay; voir la page sur l'ADN condensé). |
|
|
|
|
|
2.2.2. Les phases cellulaires, relationnelles ou sociales |
||
|
Comme pour les molécules on ne s'attache pas aux propriétés d'un ensemble d'éléments (cellules, fibres...) mais à des surfaces ou des volumes (des espaces...) dont les propriétés dynamiques viennent d'autre part que des propriétés de leurs composants. |
|
Une
première
distinction
peut se faire
selon le
critère
de
cohésion
des phases: La découverte récente de l'établissement de nanotubes entre bactéries (même de deux espèces différentes) d'une même culture me semble être une bonne occasion de s'intéresser à la géométrie (et à la dynamique) de la genèse d'un pont cytoplasmique entre deux cellules en la comparant à la dynamique (voisine) de la fusion cellulaire et enfin à celle (partiellement opposée) de la division cellulaire Les matrices cellulaires (infographie ici) tant intracellulaires qu'extracellulaires sont clairement des milieux thyxotropiques. La composition chimique - due pour les deux à l'activité cellulaire - et surtout les arrangements de l'eau en leur sein sont encore des domaines trop peu explorés. |
|
On a gardé le nom de tissu (un héritage de la théorie tissulaire) pour désigner des assemblages de cellules associées pour assurer une fonction commune. |
||
|
|
|
|
|
|
||
|
Plutôt que de se focaliser sur les types physiques on peut faire une description plus géométrique des différents tissus : |
|
L'œuf
est une boule
puis deux
types
embryonnaires
fondamentaux
se
dégagent: On observe dans certains embryons un changement de phase "boule --> plans" par exemple en cas de la formation d'une cavité (cœlome...) au sein d'un massif embryonnaire. |
|
À la suite du développement embryonnaire les géométries de base se complexifient et surtout peuvent se rompre en sous-unités qui peuvent même changer de phase. L'exemple le plus étudié est celui de la croissance ramifiante des réseaux d'échanges pulmonaires. La dimension fractale donnant lieu, par réitération, à l'arborescence bronchique. Une analogie évidente peut être faite avec les mélanges de phases entre deux fluides de densité plus ou moins voisine. Voir quelques données anatomiques et biophysiques sur la ventilation de l'homme (cours de seconde, &2.1.1) Dans le même registre voir les travaux de Vincent Fleury (Des pieds et des mains ; Genèse des formes de la nature, Flammarion, col. Champs, 2003). |
|
Dans un domaine encore bien peu exploré sous cet angle on pourrait s'efforcer de comprendre les périodes critiques embryonnaires (avec acquisition ou perte de compétence) comme des discontinuités ou des transitions de phases lors d'un développement autonome. Travaux de Rosine Chandebois (support mathématique inexistant à construire), travaux de Vincent Fleury (support mathématique élémentaire plutôt de l'ordre de l'analogie) et bien sûr travaux de René Thom (mathématiques mais sans support embryologique précis...). En travaux |
|
|
|
|
|
2.2.3. Les phases fonctionnelles ou des organes |
||
|
Ce domaine est encore moins balisé que les deux précédents. Les fonctions sont la plupart du temps considérées comme émergentes; je préférerais ici les voir comme héritables et stables pour chaque individu (sans support matériel a priori).. |
|
Le premier exemple que l'on pourrait essayer de formaliser est celui de la nutrition. On possède d'abord une assez bonne description mathématique du lacet de prédation chez Thom (et Lacorre - voir cours de Terminale Spécialité) ainsi que des considérations plus générales sur la blastula physiologique ou son équivalent chez les plantes (voir extrait d'Esquisse d'une sémiophysique dans le cours de Terminale Spécialité). |
|
Suivant l'adage, rappelé par Thom, la fonction crée l'organe, non pas au sens actuel supposé Lamarckien (voir ancien cours de TS sur l'évolution, encadré sur Lamarck, qui proposait une philosophie matérialiste mécaniciste) mais au sens de la propagation de prégnances* (voir cours de 1èreS, généralités sur les niveaux d'organisation, &2.3). Capture, digestion, absorption... sont autant de phases nutritionnelles qui peuvent reposer sur des fonctions... dont les caractéristiques peuvent expliquer les morphologies des organes. Une surface d'absorption ou d'échange entre deux milieux est contrainte par la fonction à une géométrie plus ou moins définie. |
|
*voir les 4 causes d'Aristote en SVT pour le vocabulaire thomien
En travaux |
|
|
|
2.3 Les fonctions du vivant : la vie mathématisée |
|
|
||
|
« D'une manière générale, le progrès le plus radical qu'une science puisse accomplir consiste à faire entrer les résultats déjà acquis dans un ensemble nouveau, par rapport auquel ils deviennent des vues instantanées et immobiles prises de loin en loin sur la continuité d'un mouvement. Telle est, par exemple, la relation de la géométrie des modernes à celle des anciens. Celle-ci, purement statique, opérait sur les figures un fois décrites; celle-là étudie la variation d'une fonction, c'est-à-dire la continuité du mouvement qui décrit la figure. On peut sans doute, pour plus de rigueur, éliminer de nos procédés mathématiques toute considération de mouvement; il n'en est pas moins vrai que l'introduction du mouvement dans la genèse des figures est à l'origine de la mathématique moderne. Nous estimons que, si la biologie pouvait jamais serrer son objet d'aussi près que la mathématique serre le sien, elle deviendrait à la physico-chimie des corps organisés ce que la mathématique des modernes s'est trouvée être à la la géométrie antique.» Bergson, l'Évolution créatrice, 1907, 32 |
|
Il y a, dans ce texte de Bergson un profonde résonance avec l'œuvre de Thom. Ils s'accordent dans l'importance à accorder à la notion de fonction dont j'ai déjà parlé ailleurs. |
||||
|
|
|
|
|
approche probabiliste de l'homogène versus approche individualiste (spontanée ou autonome) |
||
|
Le cytosol , vu de très loin, et avec une résolution inférieure à la distance entre les éléments d'un système macromoléculaire (que l'on pourrait chiffrer à quelques dizaines ou centaines de nanomètres), est homogène chimiquement. Mais si l'on s'approche des éléments moléculaires (à une distance inférieure à la dizaine de nanomètres) l'hétérogénéité saute aux yeux et il semble nécessaire de changer de modèle et passer à un modèle qui tienne compte de l'individualité des molécules. |
|
Du point de
vue
philosophique
deux courants
(au moins) me
semblent
pertinents
pour
comprendre
cette
individualité
: |
|
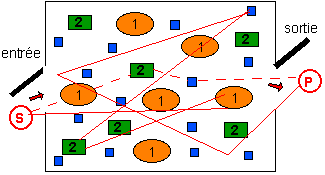
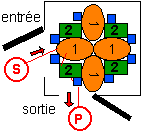
Dans le tableau ci-dessous je mets en regard deux conceptions d'un système métabolique (ou chaîne métabolique) théorique où un substrat est transformé en un produit: la vision probabiliste à gauche et la vision causale à droite. |
||
|
Ces éléments sont inspirés du chapitre 12 (L'eau, une interface hétérogène et dynamique des macromolécules) du livre de P. Mentré (L'eau dans la cellule, Pascale Mentré, 1995, Masson) mais la formulation et le développement des idées déforment peut-être la pensée de cet auteur auquel je renvoie. |
chaîne
métabolique
statistique chaîne
métabolique
finaliste *
termes
empruntés
à P.
Mentré:
Organization
and properties
of water in
cell system,
in Integrated
Plant Systems,
H. Greppin et
al., eds.,
2000,
University of
Geneva, pp
3-22 substrat
---->
système
métabolique
statistiquement
homogène
compris
comme --->
produit
substrat
----->
système
métabolique
hétérogène
composé
de: --->
produit
Remarque: |
||||||||||||||||||||||||||||||
|
|
|
|
|
fonctions locales et fonctions globales |
||
|
Voir l'extrait de Paraboles et catastrophes de René Thom dans l'ancien cours de 1èreS. |
|
Le terme de fonction a probablement une origine biologique et sociologique. Cette idée n'a été soutenue que tardivement par René Thom ( voir Analyse sémantique d'un mot polysémique: la fonction, 1993, Séminaires de la Société de Biologie Théorique, année 1992-1993, Acta Biotheoretica, 42 ). Puis la fonction a été formalisée en mathématique (dans le plan, la fonction (numérique) d'une variable (x) est représentée par un graphe y=f (x); en mathématique la représentation d'une relation de quantité (avec des variables numériques) ou de qualité entre deux ensembles d'objets est défini par le terme moderne d'application (Fréchet, 1909)). La fonction est enfin retournée dans le domaine social et dans celui de la biologie. |
|
Pour un système vivant on ne peut pas parler de fonction -au sens strictement biologique - au niveau local (fonction alcool ou déshydrogénase...; c'est pour cela, je crois, que les chimistes préfèrent maintenant employer le terme de groupe fonctionnel pour des molécules). On garder donc le terme de fonction pour des phénomènes physiologiques globaux: d'abord les grandes fonctions non locales du vivant (nutrition, relation, reproduction), puis des fonctions comme l'homéostase ou encore la fonction enzymatique. |
|
Se nourrir est une fonction homéostatique (cours de seconde) La fonction enzymatique est une fonction topologique (cours de 1èreS) |
|
|
|
|
|
application directe: le clonage |
||
|
ancienne page sur les manipulations cellulaires et le clonage
Dossier
Généthique
à
recommander:
pour la
compréhension
des enjeux: |
|
Notre compréhension du clonage repose grandement sur la théorie cellulaire. Une première alternative, suivie par exemple par Mme Chandebois (voir ses ouvrages dans la bibliographie), a été de redonner une certaine autonomie aux cellules et surtout de mieux faire comprendre que c'est avant tout l'environnement qui détermine le destin d'une cellule (et non un programme génétique interne).
|
|
Mais on peut aller nettement plus loin. Si l'on s'affranchit des limites cellulaires et que l'on veut bien regarder l'embryon comme un tout, avec les grandes fonctions non locales qui le définissent comme UN être vivant, on peut progresser dans une direction originale. |
|
Dans une vision que l'on pourrait qualifier de holiste ou fonctionnelle, un embryon au stade une cellule est totipotent parcequ'il possède la totalité des champs fonctionnels du vivant : c'est un être vivant complet. Que l'on puisse le dupliquer en altérant la fusion des premiers blastocystes aux premiers stades embryonnaires (2, 4 ,8 cellules) n'est pas non plus vraiment surprenant puisque les fonctions semblent encore peu localisées. Les cellules souches embryonnaires (stem cells) sont prélevées au stade blastocyte (100-200 cellules) et possèdent encore clairement ces fonctions globales : elles sont totipotentes. |
|
|
|
|
|
|
||
|
Pour des données sur les cellules souches (dans le cadre du paradigme moléculariste) http://www.genethique.org /doss_theme/ dossiers/ cellules_souches/ acc.cellulessouches.htm |
|
Au cours de la différenciation les fonctions deviennent de plus en plus locales et complexes dans leur géométrie (par exemple la nutrition est assurée par un appareil comprenant plusieurs organes et la fonction globale s'est en quelque sorte multipliée en sous-fonctions locales, aucune partie n'ayant la capacité de réaliser la fonction globale de nutrition). Une cellule appartenant à un organe ou plus exactement un fragment de tissu ne possède donc pas non plus une fonction globale complète. On notera en effet que l'on ne prélève pas les cellules, isolément, mais un fragment tissulaire dont on dissocie ensuite artificiellement les cellules. Les cellules manipulées sont donc plutôt des fragments tissulaires vis-à-vis des fonctions. |
|
Que signifie alors le fait que ces fragments tissulaires différenciés puissent être utilisés pour donner des tissus différents (pluripotents) ? Je doute que la totalité des fonctions du vivant puissent à nouveau être transmises par ces fragments (et puisse donc donner, par quelque traitement que ce soit, un individu complet : totipotence). D'ailleurs on peut penser que les dédifférenciations ne puissent se faire qu'entre tissus intégrés à une même fonction globale: nutrition ou relation... mais, comme les limites en sont bien difficiles à cerner, cela ne semble pas forcément une évidence. |
|
Ces fragments tissulaires peuvent être "reprogrammés", c'est-à-dire qu'ils perdent (le plus souvent à la suite d'une manipulation génétique réalisée par l'insertion de séquences virales associées à des séquences de l'organisme père) leurs caractéristiques de tissus différenciés et qu'ils peuvent donner des types tissulaires plus ou moins variés selon la manipulation génétique et les conditions de culture. Le fait que l'on ne se contente pas de modifier les conditions de culture rend l'interprétation très difficile. En effet, le sens des manipulations génétiques est toujours extrêmement difficile à déduire d'expériences qui sont basées sur des SÉLECTIONS. On sélectionne en effet des souches qui présentent telles ou telles caractéristiques vivantes. Que des gènes soient à l'origine des modifications est une hypothèse qui préexiste dans le modèle expérimental et ne peut en aucun cas être prouvé par l'expérience (voir Gérard Nissim Amzallag, La Raison malmenée :de l'origine des idées reçues en biologie moderne, 2002, CNRS Éditions). Les fragments tissulaires aux nouvelles propriétés peuvent très bien présenter ces nouvelles caractéristiques de par leur propre autonomie et pouvoir adaptatif, déclenché par les conditions expérimentales. |
|
|
|
|
|
|
|
En travaux |